

 |
 |
|
|
Навигация
Популярное
|
Публикации «Сигма-Тест» Метод вакуумного напыления 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 [ 44 ] 45 46 47 48 49 50 51 52 53 54 (CoJIigCrJ!!,)! (ВОГ )o,49ClS:,2 0o: (ОН )o.84 1.50 HO; сплав Co - 30 Cr - 20 B: (CoJ!oi CrJIIg)! (BOr )o.52 CIo3 Ом2(ОН- )o,6o -ОбНО, Как видно из этих данных, при увеличении содержания хрома в сплаве повышается и его концентрация в поверхностной пленке, что способствует улучшению защитных свойств этой пленки. При этом электрический ток активного растворения снижается и потенциал коррозии повышается. Когда содержание хрома в сплаве становится -равным 30% (ат.), в поверхностной пленке практически имеются только катионы хрома, в результате чего сплав самопассивируется, как это было описано выше. Однако в пленке, образующейся на поверхности этих сплавов, в большом количестве имеются ионы борной кислоты. В том случае, когда в состав аморфного сплава входит кремний, в поверхностной пленке содержатся соли кремниевой кислоты (силикаты) [23]. В отличие от этого, сплав Со-ЮСг-20Р, несмотря на небольшое количество хрома, самопассивируётся в 1 и. водном растворе НС1, а состав образующейся пассивирующей пленки может быть описан как (ColisСт1%)г (РО]- )о,озCli О (ОН-)2,8б ;с -0.30) НО. В сплавах, имеющих в своем составе фосфор и хром, который при естественной коррозии быстро накапливается в поверхностной пленке, ионы фосфорной кислоты в пленке почти не содержатся. Следовательно, можно предположить, что эта пленка почти полностью состоит из гидратированного оксида-гидрооксида хрома. Для сплавов, содержащих хром, концентрация хрома в гидра-тированном оксиде-гидрооксиде хрома в возникающей на поверхности сплава пассивирующей пленке высока, что улучшает защитные свойства этой пленки. Об этом уже говорилось. Если в аморфных сплавах имеются бор и кремний, то они проникают в поверхностную пленку, превращаясь соответственно в бораты и силикаты хрома, при этом концентрация хрома в гидратированном оксиде - гидроксиде хрома в поверхностной пленке невелика. Несмотря на то, что в аморфных сплавах Со-25Сг-25В и Со-ЮСг-20Р концентрация хрома в поверхностной пленке в виде положительных ионов при естественной коррозии превышает 80%. первый сплав находится в активном состоянии, а второй самопассивируется. Это происходит вследствие того, что содержание бората хрома и концентрация гидратированного оксида - гидрооксида хрома в возникающей на поверхности первого сплава пленке недостаточно велики. Вероятно, довольно трудно повысить коррозионную стойкость аморфных сплавов, содержащих бор и кремний, по отношению к коррозионной стойкости аморфных сплавов с фосфором. Как уже говорилось, фосфор, содержащийся в аморфных сплавах типа металл - металлоид, способствует ускоренному формированию пассивирующей пленки. Это происходит благодаря тому, что фосфор ускоряет активное растворение сплава, что приводит к накоплению в пленке металлических элементов, повышающих ее защитные характеристики, а ионы фосфорной кислоты практически выводятся из пленки. Фосфор является наиболее эффективным элементом для повышения коррозионной стойкости аморфных сплавов, содержащих металлы типа хрома как второй металлический компонент. Так, из рис. 9.12 видно, что коррозионная стойкость аморфных сплавов Ti-Си существенно повышается при добавлении небольших количеств фосфора. Углерод, содержащийся в аморфных сплавах, не проникает в поверхностную пленку и поэтому ой не оказывает такого же ускоряющего воздействия на активное растворение, как фосфор. Иными словами, с точки зрения повышения коррозионной стойкости, углерод не достаточно эффективен при введении его в аморфный сплав совместно с хромом-. Бор и кремний так же, как и углерод, слабо ускоряют активное растворение аморфных сплавов. Бор и кремний не способствуют накоплению на поверхности раздела сплав/раствор элементов, эффективно влияющих на образование защитной пленки, поэтому, особенно в водных растворах сильных кислот, несмотря на проникновение этих элементов в возникающую поверхностную пленку в качестве боратов и силикатов, они оказывают слабое воздействие на ускорение формирования такой пленки. 9.3.3. Химическая гомогенность сплавов В тех случаях, когда пассивирующая пленка образуется достаточно быстро, коррозионная стойкость сплава определяется тем, насколько однородно протекает ее образование. В этом отношении аморфные сплавы характеризуются превосходно. Как указывалось в главе 4, при термической обработке аморфных сплавов типа металл - металлоид в исходной аморфной матрице последовательно возникает несколько метастабильных кристаллических фаз, после чего структура становится стабильно кристаллической. При термической обработке с кристаллизацией изменяется , также и коррозионное поведение аморфных сплавов, иллюстрацией чему может служить рис. 9.19 [24]. На рисунке показаны изменения вида потёнциодинамических кривых анодной поляризации в 1 н. водном растворе НС1 аморфного сплава Fe-ЮСг-13Р-7С в зависимости от продолжительности термической обработки при 430°С. Выше уже говорилось о том, что дан- Существует также миеиие, что роль углерода в формировании оксидной пленки ие столь уж скромна и что углерод может значительно улучшить коррозионные свойства аморфных сплавов. Так, в [47]* показано, что коррозионная стойкость сплава Fe-Сг-Р-С значительно выше стойкости сплава Fe- Сг-Р; присутствие углерода улучшает параметры пассивации иа два порядка. Такое благоприятное влияние углерода иа процесс пассивации связывают с образованием иа поверхности аморфного сплава химически стойких комплексов с карбофосфидиой координацией атомов [43 44]*. Прим. ред. 9* Зак. 307
ный аморфный сплав самопассивируется в 1 н. водном растворе НС1. Потенциал коррозии резко снижается, как только в исходной аморфной фазе появляются метастабильные кристаллические фазы, в результате чего пассивирующая пленка распадается и сплав переходит в активное состояние. Одновременно резко возрастает плотность тока анодного растворения. По мере протекания кристаллизации электрический ток продолжает возрастать. В аморфных сплавах железо - металлоид при термической обработке при 350°С метастабильные кристаллические фазы появляются только при очень длительном отжиге продолжительностью несколько месяцев. При этом диаметр кристаллитов, выпадающих из пе1ресы-щецной исходной аморфной фазы, составляет ~10 нм. Хотя средний химический - состав кристаллитов пересыщенного твердого раствора отвечает составу исходной аморфной фазы, но вследствие выделения кристаллической фазы коррозионная стойкость сплава снижается до уровня, близкого к уровню коррозионной стойкости на заключительной стадии кристаллизации, т. е. после высокотемпературной термической обработки [20]. Быстрое охлаждение повышает коррозионную стойкость кристаллических сплавов. Если сравнить коррозионную стойкость кристаллического СПлава, полученного медленным охлаждением, п однофазного твердого кристаллического раствора, полученного быстрым охлаждением из расплава, то можно заметить, что во втором случае коррозионная стойкость значительно выше. На рис. 9.20 приведены кривые анодной поляризации в 1 н. водном растворе НС1 кристаллических сплавов Ti-N, полученных обычными способами охлаждения и закаленных из расплава; показана также поляризационная кривая аморфного сплава [25]. Видно, что быстрое охлаждение является эффективным средством повышения коррозионной стойкости кристаллических сплавов. Аналогичный вывод сделан в работе [26] на основании эксперямен- -15 О 0,5 1,0 1,5 2,0 Рис. 9.19. Изменение вида потен-Цйодииамических кривых анодной поляризации аморфного сплава Fe-ЮСг-13Р-7С (1 н. водный раствор НС1) в зависимости от продолжительности термической обработки при 430°С (цифры у кривых - время термической обработки, мии): /4 - сплав до термической обработки 1 Изменение параметров пассивации и коррозионной стойкости (на 2-3 порядка) возможно также в результате протекания процессов структурной релаксации в рамках рентгеновски аморфного состояния [21]*. Прим. ред. \ 10 тальных результатов, показывающих, что расплавленный лазерным лучом поверхностный слой, например кристаллической аустенитиой нержавеющей стали, имеет крайне высокую коррозион. ную стойкость по сравнению с той же сталью, не обработанной лазером. Хорошо известно, что границы зерен в кристаллических сплавах являются участками облегченного возникновения коррозии. Кристаллические сплавы, закаленные из жидкого состояния, состоят из очень 1иелких кристаллитов и поэтому удельная поверхность границ зерен в -них очень велика по сравнению со сплавами, полученными опособамп охлаждения. Однако тот факт, что коррозионная стойкость быстрозакаленных кристаллических сплавов значительно выше, чем медленно охлажденных сплавов, свидетельствует от том, что границы кристаллитов в быстрозакаленных сплавах не оказывают существенного влияния на их коррозионное поведение, поскольку в процессе быстрого охлаждения из рас плава не возникают флуктуации химического состава, облегчающие коррозию. Следовательно, сплавы, полученные путем быстрого охлаждения жидкости, хоть и являются, кристаллическими, но не имеют локальных колебаний химического состава на таких дефектах, как границы кристаллитов, т. е. характеризуются высокой химической гомогенностью. Если такие колебания химического состава не появляются и при последующей термической обработке, то сплав имеет превосходную коррозионную стойкость. Напротив, когда аморфные сплавы кристаллизуются при термической обработке, то, хотя между отдельными кристаллитами и нет различий в химическом составе, есть отличие между их химическим составом и Составом исходной аморфной фазы, что нарушает химическую гомогенность сплава. Эти колебания состава проявляются прежде всего по содержанию хрома в окрестности межфазных границ. Обобщая сказанное, можно подчеркнуть следующее. В кристаллических сплавах такие дефекты, как фазовая неоднородность, сегрегации, выделения и т. п., сопровождающиеся колебаниями 0,5 1,0 1,5 2,0 Потеноиш1,о. Рис. 9.20. Кривые анодной поляризации кристаллических сплавов Ti-N1, полученных обычным охлаждением и закалкой из. расплава, а также аморфного сплава Ti-N1-Р в 1 н. водном растворе НС1: 1 - кристаллический сплав Ti- 61,5Ni; 2 - кристаллический сплав Ti-40Ni; 3 - быстрозакалеиный кристаллический сплав Ti-61,5Ni; 4 - быстрозакалеиный кристаллический сплав Ti-40Ni; 5 - аморфный сплав Ti-56,5№-5Р химического состава, являются центрами зарождения коррозии, так как именно здесь не образуется устойчивая пассивирующая пленка, что, собственно, и облегчает коррозию. В аморфных сплавах отсутствуют как дефекты кристаллического строения, так и дефекты, обусловленные протеканием диффузии атомов твердого раствора, которая подавляется при быстром охлаждении. Следовательно, аморфные сплавы не содержат и дефектов, вызывающих локальные колебания химического состава, т. е. они являются химически однородными однофазными твердыми растворами. Это способствует образованию однородной пассивирующей пленки и, в конечном счете, определяет их высокую коррозионную стойкость. 9.4. ВЛИЯНИЕ ЛЕГИРУЮЩИХ МЕТАЛЛИЧЕСКИХ ЭЛЕМЕНТОВ Из данных, приведенных на рис. 9.2-9.4, можно видеть, какие металлические элементы повышают коррозионную стойкость аморфных еплавов типа металл - металлоид. Степень повышения потенциала коррозии и снижения анодного тока зависит от того, какой элемент вводится в сплав в качестве второго металлического компонента. Повышение потенциала коррозии и снижение анодного тока соответствует уменьшению скорости свободной коррозии Аморфные сплавы, не содержащие второго металлического элемента, в различных средах обычно не пассивируются, но при введении второго металлического элемента эти сплавы обычно переходят в пассивное состояние именно за счет анодной поляризации. Величина эффекта такого легирования зависит от соотношения активностей легирующего металла и металла основы сплава [27]. 9.4.1. Случай, когда легирующий элемент более активен, чем металл основы сплааа В аморфные сплавы металл - металлоид в качестве активных легирующих добавок вводят Ti, Zr, V, Nb, Та, Сг, Мо, W. Влияние на коррозию в активном состоянии Аморфные сплавы металл - металлоид, содержащие большие количества хрома или титана, самопассивируются, при этом скорость коррозии, естественно, становится крайне низкой. Однако, если такие металлические элементы, большие концентрации которых приводят к самопассивации, содержатся не в достаточных количествах, сплав оказывается активным. Аналогичным образом на скорость коррозии влияют и другие вышеперечисленные металлы. На рис. 9.21 приведены потенциодинамические кривые анодной поляризации в 1 н. водном растворе НС1 в случае введения различных количеств молибдена в аморфный сплав Fe-13Р-7С [28]. Легирование молибденом снижает скорость активного растворения, т. е. скорость коррозии сплава. Данные РФС о химическом составе поверхностной пленки, образующейся в этих сплавах при различных потенциалах, приведены на рис. 9.22 [2]. На этом ри-. сунке показана концентрация положительных ионов в поверхностной пленке l[Mo]/(![Fe]!+i[Mo]), i[Fe]/([Fe] + [Mo]) как функция потенциала поляризации. Видно, что- пленка, образующаяся тогда, когда сплав находится в активном состоянии, содержит значительные количества молибдена. Такая же тенденция обнаруживается и при добавлении других металлических элементов в больших количествах [27]. Интересно, что накопление в поверхностной пленке, образующейся в активном состоянии, элементов, более активных, чем основа, характерно не только для аморфных сплавов. Например, молибден в больших количествах накапливается также в пленке, возникающей в активном состоянии на поверхности нержавеющей стали, содержащей молибден [30]. 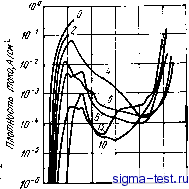 40,2 О
-0,5 О 0,5 1,0 1,5 2,0 2,5 Потенциал, д , Рис. 9.21. Потенциодинамические кривые анодной поляризации аморфных сплавов Fe-Мо-I3P- 7С в 1 и. водном растворе HCI [цифры у кривых - содержание молибдена, % (ат.)] u,L и,ч и,и и,и Лотенциа/!,8 Рис. 9.22. Концентрация катионов в поверхностной пленке аморфных сплавов Fe-Мо-13Р-7С при по-тенциостатической поляризации при выдержке в течение 1 ч в 1 и. водном растворе НС1: 1 - Fe-8Мо- 1 ЗР-7с; 2 - Fe- ЮМо-13Р-7С; 3 -Fe-15Мо- 13Р-7С Потенциалы активного растворения сплавов на оснрве железа, кобальта и никеля, в частности в сильных окислительных средах, повышаются при добавлении перечисленных выше металлов, обладающих большей активностью, чем металлы основы. При этом сплав обычно переходит в пассивное состояние. Если происходит активное растворение сплава, то активные легирующие элементы в больших количествах накапливаются в химических продуктах коррозии, которые образуют довольно толстую пленку (порядка нескольких нанометров). Эта пленка выполняет роль барьера \лл диффузии ионов металла, участвующих в растворении сплава, т. е. Предложенное авторами объяснение защитного действия молибдена следует рассматривать как дискуссионное, поскольку оно не согласуется с данны- ми ряда работ, полученных на кристаллических материалах [11, 57}*). Ярил. ред. (см. например,
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
© 2010 www.sigma-test.ru Санкт-Петербург: +7 (812) 265-34-48, +7 (812) 567-94-10
Разработка и поддержка сайта: +7(495)795-01-39 после гудка 148651, sigma-test.ru(my_love_dog)r01-service.ru Копирование текстовой и графической информации разрешено при наличии ссылки. |